АХМЕТОВ М. А. УРОК 10. ЗАДАНИЯ Выбрать другой урок
Характеристика переходных элементов – меди, хрома, железа по их положению в периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов.
1. Атомы каких элементов имеют по 1 электрону на внешнем занятом электронном уровне в основном состоянии?
|
1)
|
Fе и Zn
|
|
2)
|
Zn и Cr
|
|
3)
|
Cr и Cu
|
|
4)
|
Cu и Fe
|
2. Для получения хрома из его оксида в роли восстановителя используют
|
1)
|
алюминий и кремний
|
|
2)
|
кремний и водород
|
|
3)
|
водород и углерод
|
|
4)
|
углерод и алюминий
|
3. Железо не получают по реакции
|
1)
|
3FeO + 2Al 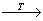 Al2O3 + 3Fe Al2O3 + 3Fe
|
|
2)
|
электролизом раствора сульфата железа по уравнению
FeSO4 + 2H2O ® Fe + H2 + O2 + H2SO4
|
|
3)
|
восстановлением коксом FeO + C 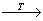 Fe + CO Fe + CO
|
|
4)
|
восстановлением серой 2FeO + S 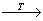 2Fe + SO2 2Fe + SO2
|
4. Реакция, не происходящая в доменном процессе
|
1)
|
CO2 + C = 2CO
|
|
2)
|
3Fe2O3 +CO 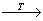 2Fe3O4+ CO2 2Fe3O4+ CO2
|
|
3)
|
3FeO + CO2 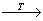 Fe3O4+ CO Fe3O4+ CO
|
|
4)
|
Fe3O4 + CO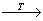 3FeO + CO2 3FeO + CO2
|
5. Латунь – это сплав меди с
|
1)
|
цинком
|
|
2)
|
оловом
|
|
3)
|
никелем
|
|
4)
|
хромом
|
6. Раствор хлорида железа (III) реагирует с веществами, формулы которых
|
1)
|
Cu и KI
|
|
2)
|
KI и FeCl2
|
|
3)
|
FeCl2 и Ag
|
|
4)
|
Ag и Cu
|
7. Хромат калия в химической лаборатории можно получить действием на хромит калия
|
1)
|
пероксидом водорода в щелочной среде и хлором в кислой среде
|
|
2)
|
пероксидом водорода в щелочной среде и хлором в щелочной среде
|
|
3)
|
пероксидом водорода в кислой среде и хлором в щелочной среде
|
|
4)
|
пероксидом водорода в кислой среде и хлором в кислой среде
|
8. Выберите наиболее справедливое окончание следующего утверждения
«При добавлении к раствору хромата калия серной кислоты …
|
1)
|
хромат превращается в хромит и окраска изменяется с оранжевой на желтую
|
|
2)
|
хромат превращается в хромит и окраска изменяется с желтой на оранжевую
|
|
3)
|
хромат превращается в дихромат и окраска изменяется с оранжевой на желтую
|
|
4)
|
хромат превращается в дихромат и окраска изменяется с желтой на оранжевую
|
9. Смесь дихромата калия и концентрированной серной кислоты нередко называют хромовой смесью. Заменять концентрированную серную кислоту на концентрированную соляную кислоту нельзя, потому, что
|
1)
|
максимальная массовая доля HCl в соляной кислоте составляет 38%, а серная кислота бывает полностью безводной
|
|
2)
|
соляная кислота сама реагирует с дихроматом калия по уравнению
K2Cr2O7 +14HCl ® 3Cl2 + 2CrCl3 + 2KCl + 7H2O
|
|
3)
|
серная кислота обладает водоотнимающими свойствами, а соляная кислота – нет
|
|
4)
|
концентрированная серная кислота проявляет окислительные свойства, а концентрированная соляная кислота – нет
|
10. Гидроксид хрома (III) проявляет амфотерный характер, следовательно он растворяется
|
1)
|
в воде и бензоле
|
|
2)
|
бензоле и соляной кислоте
|
|
3)
|
соляной кислоте и растворе гидроксида натрия
|
|
4)
|
растворе гидроксида натрия и воде
|
11. Гидроксид железа (II) на воздухе
|
1)
|
разлагается с образованием FeO
|
|
2)
|
на воздухе легко окисляется до Fe(OH)3
|
|
3)
|
реагирует с парами воды, образуя кристаллогидрат Fe(OH)3·n(H2O)
|
|
4)
|
разлагается с образованием Fe2O3
|
12. Качественная реакция на FeCl3 + NH4SCN ® является
|
1)
|
необратимой, так как при добавлении к раствору новой порции тиоционата аммония наблюдается усиление красной окраски
|
|
2)
|
обратимой, так как с течением времени красный цвет раствора исчезает
|
|
3)
|
обратимой, так как при добавлении к полученному раствору гидроксида натрия красная окраска исчезает и образуется бурый осадок гидроксида железа (III)
|
|
4)
|
необратимой потому, что осадок со временем оседает на дно пробирки
|
13. В химической лаборатории оксид хрома (III) получают разложением каждого из двух веществ, формула которых
|
1)
|
(NH4)2Cr2O7 и K2Cr2O7
|
|
2)
|
K2Cr2O7 и K2CrO4
|
|
3)
|
K2CrO4 KCrO2
|
|
4)
|
KCrO2 и (NH4)2CrO4
|
14. Оксид хрома (VI) можно получить в результате взаимодействия этих веществ с концентрированной серной кислотой
|
1)
|
K2Cr2O7 и Cr2O3
|
|
2)
|
Cr2O3 и Cr
|
|
3)
|
Cr и K2CrO4
|
|
4)
|
K2CrO4и K2Cr2O7
|
15. Оксид хрома (III) входит в состав абразивных материалов (паст ГОИ), так как его кристаллическая решетка
|
1)
|
молекулярная
|
|
2)
|
ионная
|
|
3)
|
атомная
|
|
4)
|
металлическая
|
16. Оксид хрома (III) реагирует с каждым из двух веществ
|
1)
|
кальцием и алюминием
|
|
2)
|
алюминием и серебром
|
|
3)
|
серебром и чугуном
|
|
4)
|
чугуном и кальцием
|
17. Оксид хрома (VI) не реагирует с веществом, формула которого
|
1)
|
С2Н5ОН
|
|
2)
|
Mn2O7
|
|
3)
|
Cr
|
|
4)
|
CH3CHO
|
18. Формула карбида железа (цементита)
|
1)
|
FeC2
|
|
2)
|
Fe3C
|
|
3)
|
Fe4C3
|
|
4)
|
Fe2C3
|
19. Установите продукт взаимодействия в следующей химической реакции, учитывая, что образуется вещество голубовато-зеленого цвета
Cu2O + CO2 + O2 + H2O ®
|
1)
|
Cu(HCO3)2
|
|
2)
|
Cu2CO3
|
|
3)
|
(CuOH)2CO3
|
|
4)
|
CuCO3
|
20. При взаимодействии концентрированной серной кислоты с хлоридом железа (II) образуются
|
1)
|
сульфат железа (III) + диоксид серы + хлороводород + вода
|
|
2)
|
сульфат железа (II) + хлороводород + вода
|
|
3)
|
сульфат железа (III) + диоксид серы + хлор + вода
|
|
4)
|
сульфат железа (II) + хлор + вода
|
21. Установите соответствие между химическими элементами и проявляемыми ими степенями окисления
|
|
ХИМИЧЕСКИЕ ЭЛЕМЕНТ
|
|
СТЕПЕНИ ОКИСЛЕНИЯ
|
|
1)
|
Zn
|
А)
|
0, +2, +4, +6
|
|
2)
|
Cr
|
Б)
|
0,+1,+2,+3, +6
|
|
3)
|
Mn
|
В)
|
0, +2, +3, +4, +5, +6, +7
|
|
4)
|
Fe
|
Г)
|
0, +2
|
|
|
|
Д)
|
0,+2, +3, +6
|
22. Установите соответствие между химическим элементом и числом неспаренных электронов в его атоме
|
|
ХИМИЧЕСКИЕ ЭЛЕМЕНТ
|
|
ЧИСЛО НЕСПАРЕННЫХ
|
|
1)
|
Сr
|
А)
|
1
|
|
2)
|
Cu
|
Б)
|
3
|
|
3)
|
Mn
|
В)
|
4
|
|
4)
|
Fe
|
Г)
|
5
|
|
|
|
Д)
|
6
|
23. Установите соответствие между формулой вещества и его окраской
|
|
ХИМИЧЕСКИЕ ЭЛЕМЕНТ
|
|
ЧИСЛО НЕСПАРЕННЫХ
|
|
1)
|
CuSO4·5H2O
|
А)
|
фиолетовый
|
|
2)
|
KMnO4
|
Б)
|
голубой
|
|
3)
|
Cr2O3
|
В)
|
белый
|
|
4)
|
ZnO
|
Г)
|
зеленый
|
|
|
|
Д)
|
красный
|
24. Установите соответствие между реагентами и хромосодержащим продуктом химической реакции
|
|
РЕАГЕНТЫ
|
|
ПРОДУКТЫ
|
|
1)
|
Сr + HCl ®
|
А)
|
Cr2(SO4)3
|
|
2)
|
Cr + Cl2®
|
Б)
|
CrCl2
|
|
3)
|
Cr+ H2SO4(разб.) ®
|
В)
|
CrCl3
|
|
4)
|
Cr + H2SO4(конц.) ®
|
Г)
|
CrO3
|
|
|
|
Д)
|
CrSO4
|
25. Окрашены в красный цвет
|
А)
|
CrO3
|
|
Б)
|
FeCl3
|
|
В)
|
Cu2O
|
|
Г)
|
MnO2
|
|
Д)
|
Сr(OH)2
|
|
Е)
|
Fe(SCN)3
|
26. Веществами X1, X2, X3 в следующей цепочке превращений являются
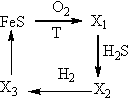
|
А)
|
SO2
|
|
Б)
|
SO3
|
|
В)
|
S
|
|
Г)
|
H2S
|
|
Д)
|
H2SO3
|
|
Е)
|
H2SO4
|

