|
Виртуальная химическая школа |
|
Химия+методика+психология Простые вещества-неметаллы |



ФТОР И ЕГО СОЕДИНЕНИЯ
Фтор F2 - открыл А. Муассан в 1886 г.
Физические свойства
Газ светло-желтого цвета; t°пл.= -219°C, t°кип.= -183°C.
Получение
Электролиз расплава гидрофторида калия KHF2:
2F- - 2ē ® F20
Химические свойства
F2 - самый сильный окислитель из всех веществ:
2F2 + 2H2O ® 4HF + O2 H2 + F2 ® 2HF (со взрывом) Cl2 + F2 ® 2ClF
Фтористый водород
Физические свойства
Бесцветный газ, хорошо растворим в воде t°пл. = - 83,5°C; t°кип. = 19,5°C;
Получение
CaF2 + H2SO4(конц.) ® CaSO4 + 2HF
Химические свойства
Раствор HF в воде - слабая кислота (плавиковая):
HF « H+ + F-
Соли плавиковой кислоты - фториды
Плавиковая кислота растворяет стекло:
SiO2 + 4HF ® SiF4+ 2H2O
SiF4 + 2HF ® H2[SiF6] гексафторкремниевая кислота |
||
ХЛОР И ЕГО СОЕДИНЕНИЯ
Хлор Cl2 - открыт К. Шееле в 1774 г.
Физические свойства
Газ желто-зеленого цвета, t°пл. = -101°C, t°кип. = -34°С.
Получение
Окисление ионов Cl- сильными окислителями или электрическим током:
MnO2 + 4HCl ® MnCl2 + Cl2 + 2H2O 2KMnO4 + 16HCl ® 2MnCl2 + 5Cl2 + 2KCl + 8H2O K2Cr2O7 + 14HCl ® 2CrCl3 + 2KCl + 3Cl2 + 7H2O
электролиз раствора NaCl (промышленный способ):
2NaCl + 2H2O ® H2 + Cl2 + 2NaOH
Химические свойства
Хлор - сильный окислитель.
Реакции с металлами: 2Na + Cl2 ® 2NaCl Ni + Cl2 ® NiCl2 2Fe + 3Cl2 ® 2FeCl3
Реакции с неметаллами: H2 + Cl2 –hn® 2HCl 2P + 3Cl2 ® 2PClЗ
Реакция с водой: Cl2 + H2O « HCl + HClO
Реакции со щелочами: Cl2 + 2KOH –5°C® KCl + KClO + H2O 3Cl2 + 6KOH –40°C® 5KCl + KClOЗ + 3H2O Cl2 + Ca(OH)2 ® CaOCl2(хлорная известь) + H2O
Вытесняет бром и йод из галогеноводородных кислот и их солей.
Cl2 + 2KI ® 2KCl + I2 Cl2 + 2HBr ® 2HCl + Br2 Соединения хлора
|
|
|
Физические свойства
Устойчива только в водных растворах.
Получение
Ba (ClO3)2 + H2SO4 ® 2HClO3 + BaSO4¯
Химические свойства
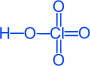
HClO3 - Сильная кислота и сильный окислитель; соли хлорноватой кислоты - хлораты:
6P + 5HClO3 ® 3P2O5 + 5HCl
HClO3 + KOH ® KClO3 + H2O
KClO3 - Бертоллетова соль; ее получают при пропускании хлора через подогретый (40°C) раствор KOH:
3Cl2 + 6KOH ® 5KCl + KClO3 + 3H2O
Бертоллетову соль используют в качестве окислителя; при нагревании она разлагается:
4KClO3 –без кат® KCl + 3KClO4
2KClO3 –MnO2 кат® 2KCl + 3O2
Хлорная кислота HCl+7O4
|
|
Физические свойства
Бесцветная жидкость, t°кип. = 25°C, t°пл.= -101°C.
Получение
KClO4 + H2SO4 ® KHSO4 + HClO4
Химические свойства
HClO4 - очень сильная кислота и очень сильный окислитель; соли хлорной кислоты - перхлораты.
HClO4 + KOH ® KClO4 + H2O
При нагревании хлорная кислота и ее соли разлагаются:
4HClO4 –t°® 4ClO2 + 3O2 + 2H2O
KClO4 –t°® KCl + 2O2
БРОМ И ЕГО СОЕДИНЕНИЯ
Бром Br2 - открыт Ж. Баларом в 1826 г.
Физические свойства
Бурая жидкость с тяжелыми ядовитыми парами; имеет неприятный запах; r= 3,14 г/см3; t°пл. = -8°C; t°кип. = 58°C.
Получение
Окисление ионов Br - сильными окислителями:
MnO2 + 4HBr ® MnBr2 + Br2 + 2H2O
Cl2 + 2KBr ® 2KCl + Br2
Химические свойства
В свободном состоянии бром - сильный окислитель; а его водный раствор - "бромная вода" (содержащий 3,58% брома) обычно используется в качестве слабого окислителя.
Реагирует с металлами:
2Al + 3Br2 ® 2AlBr3
Реагирует с неметаллами:
H2 + Br2 « 2HBr
2P + 5Br2 ® 2PBr5
Реагирует с водой и щелочами :
Br2 + H2O « HBr + HBrO
Br2 + 2KOH ® KBr + KBrO + H2O
Реагирует с сильными восстановителями:
Br2 + 2HI ® I2 + 2HBr
Br2 + H2S ® S + 2HBr
Бромистый водород HBr
Физические свойства
Бесцветный газ, хорошо растворим в воде; t°кип. = -67°С; t°пл. = -87°С.
Получение
2NaBr + H3PO4 –t°® Na2HPO4 + 2HBr
PBr3 + 3H2O ® H3PO3 + 3HBr
Химические свойства
Водный раствор бромистого водорода - бромистоводородная кислота еще более сильная, чем соляная. Она вступает в те же реакции, что и HCl:
Диссоциация:
HBr « H+ + Br -
С металлами, стоящими в ряду напряжения до водорода:
Mg + 2HBr ® MgBr2 + H2
с оксидами металлов:
CaO + 2HBr ® CaBr2 + H2O
с основаниями и аммиаком:
NaOH + HBr ® NaBr + H2O
Fe(OH)3 + 3HBr ® FeBr3 + 3H2O
NH3 + HBr ® NH4Br
с солями:
MgCO3 + 2HBr ® MgBr2 + H2O + CO2
AgNO3 + HBr ® AgBr¯ + HNO3
Соли бромистоводородной кислоты называются бромидами. Последняя реакция - образование желтого, нерастворимого в кислотах осадка бромида серебра служит для обнаружения аниона Br - в растворе.
HBr - сильный восстановитель:
2HBr + H2SO4(конц.) ® Br2 + SO2 + 2H2O
2HBr + Cl2 ® 2HCl + Br2
Из кислородных кислот брома известны слабая бромноватистая HBr+1O и сильная бромноватая HBr+5O3.
ИОД И ЕГО СОЕДИНЕНИЯ
Йод I2 - открыт Б. Куртуа в 1811 г.
Физические свойства
Кристаллическое вещество темно-фиолетового цвета с металлическим блеском.
r= 4,9 г/см3; t°пл.= 114°C; t°кип.= 185°C. Хорошо растворим в органических растворителях (спирте, CCl4).
Получение
Окисление ионов I- сильными окислителями:
Cl2 + 2KI ® 2KCl + I2
2KI + MnO2 + 2H2SO4 ® I2 + K2SO4 + MnSO4 + 2H2O
Химические свойства
c металлами:
2Al + 3I2 ® 2AlI3
c водородом:
H2 + I2 « 2HI
с сильными восстановителями:
I2 + SO2 + 2H2O ® H2SO4 + 2HI
I2 + H2S ® S + 2HI
со щелочами:
3I2 + 6NaOH ® 5NaI + NaIO3 + 3H2O
Иодистый водород
Физические свойства
Бесцветный газ с резким запахом, хорошо растворим в воде, t°кип. = -35°С; t°пл. = -51°С.
Получение
I2 + H2S ® S + 2HI
2P + 3I2 + 6H2O ® 2H3PO3 + 6HI
Химические свойства
Раствор HI в воде - сильная йодистоводородная кислота:
HI « H+ + I-
2HI + Ba(OH)2 ® BaI2 + 2H2O
Соли йодистоводородной кислоты - йодиды (др. реакции HI см. св-ва HCl и HBr)
HI - очень сильный восстановитель:
2HI + Cl2 ® 2HCl + I2
8HI + H2SO4(конц.) ® 4I2 + H2S + 4H2O
5HI + 6KMnO4 + 9H2SO4 ® 5HIO3 + 6MnSO4 + 3K2SO4 + 9H2O
Идентификация анионов I- в растворе:
NaI + AgNO3 ® AgI¯ + NaNO3
HI + AgNO3 ® AgI¯ + HNO3
Образуется темно-желтый осадок йодида серебра, нерастворимый в кислотах.
Кислородные кислоты йода
Йодноватая кислота HI+5O3
Бесцветное кристаллическое вещество, t°пл.= 110°С, хорошо растворимое в воде.
Получают:
3I2 + 10HNO3 ® 6HIO3 + 10NO + 2H2O
HIO3 - сильная кислота (соли - йодаты) и сильный окислитель.
Йодная кислота H5I+7O6
Кристаллическое гигроскопичное вещество, хорошо растворимое в воде, t°пл.= 130°С.
Слабая кислота (соли - перйодаты); сильный окислитель.