|
Виртуальная химическая школа |
|
Химия+методика+психология Кислород и его соединения |




КИСЛОРОД
Кислород O2 (К.В. Шееле 1772 г., Дж. Пристли 1774 г.)
Самый распространенный элемент на Земле; в воздухе - 21% по объему; в земной коре - 49% по массе; в гидросфере - 89% по массе; в составе живых организмов-- до 65% по массе.
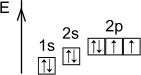
Строение атома |
||||
|
|
||||
Физические свойства
Газ - без цвета, вкуса и запаха; в 100V H2O растворяется 3V O2 (н.у.); t°кип= -183°С; t°пл = -219°C; d по воздуху = 1,1.
Способы получения
Промышленный способ (перегонка жидкого воздуха). Лабораторный способ (разложение некоторых кислородосодержащих веществ)
2KMnO4 –t°® K2MnO4 + MnO2 + O2 2KClO3 –t°;MnO2® 2KCl + 3O2 2H2O2 –MnO2® 2H2O + O2
Способы собирания |
||||
|
|
||||
Химические свойства
Взаимодействие веществ с кислородом называется окислением. С кислородом реагируют все элементы, кроме Au, Pt, He, Ne и Ar, во всех реакциях (кроме взаимодействия со фтором) кислород - окислитель.
С неметаллами C + O2 ® CO2 S + O2 ® SO2 2H2 + O2 ® 2H2O
С металлами 2Mg + O2 ® 2MgO 2Cu + O2 –t°® 2CuO
Со сложными веществами 4FeS2 + 11O2 ® 2Fe2O3 + 8SO2 2H2S + 3O2 ® 2SO2 + 2H2O CH4 + 2O2 ® CO2 + 2H2O
Горение в кислороде |
||||
|
|
||||
Озон O3
Озон -аллотропная модификация кислорода.
Физические свойства
Газ, запах свежей хвои, бесцветный, растворим в воде; t°кип= -112°С; t°пл= -193°C.
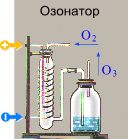
Получение
3O2 ® 2O3
Во время грозы (в природе), (в лаборатории) в озонаторе |
||||
|
|
||||
|
Действием серной кислоты на пероксид бария
3BaO2 + 3H2SO4 ® 3BaSO4 + 3H2O + O3
Химические свойства
Неустойчив: O3 ® O2 + O
2. Сильный окислитель: 2KI + O3 + H2O ® 2KOH + I2 + O2
Обесцвечивает красящие вещества, отражает УФ - лучи, уничтожает микроорганизмы. |
||||
|
|
||||
|
|
||||
|
|
||||
|
|